Destilasyon (Damıtma) Nedir? Kaça Ayrılır? Ne İşe Yarar?
Destilasyon (Damıtma) Nedir?
İki farklı bileşimin bulunması halinde gerçekleşecek destilasyon işlemi kimya biliminde kullanılır. Aynı karışım içerisindeki farklı bileşenlere göre yapılan işlemlerle ayrışmanın sağlanması amaçlanır. Damıtma olarak da adlandırılması söz konusu olurken 5 farklı çeşidi mevcuttur. Bu çeşitleri de yazı içinde değindik.
Destilasyon Ne İşe Yarar?
Organik yapıya sahip olan bileşiklerin birbirinden ayrılabilmesi için destilasyon kullanımı gereklidir. Bu sayede kolaylıkla ayrışma elde edilir. Kaynama noktasına ulaşmış olan sıvıya verilecek fazla ısı enerjisi ise buhar haline dönüşümü tamamlamasına neden olur. Sıvının tamamen işlemle gaz haline dönüşümü gerçekleşir. Sıvıya verilen ısının değişimi ise söz konusu değildir. Aynı düzeydeki ısı sayesinde belirli bir düzen içinde destilasyon kullanımıyla sıvı maddelerin ayrışması tamamlanır. Var olan madde özelliklerine göre ayrışmanın sağlanması destilasyon faydaları nelerdir sorusuna verilebilecek en iyi yanıt durumundadır.
Ayrıca Bakınız: Louis Pasteur Kimdir? Hayatı, Buluşları Nelerdir?
Kaynama noktalarının yakın olması ya da ürün özelliklerine göre gerçekleştirilecek işlemler farklılık gösterir. Bunların dışında istenen ayrışmalar özelinde de yapılacak işlemlerde farklılık olması mümkündür. Besleme akımı çerçevesinde dolgulu veya raflı kolon uygulamaları olduğu da bilinir. Daha kompleks bir şekilde gerçekleştirilen destilasyon işleminin aynı düzeyde birden fazla uygulanması da olabilmektedir. Karışımda var olan bileşen sayısına göre aynı şekillerde destilasyon işlemleri devam ettirilebilir.
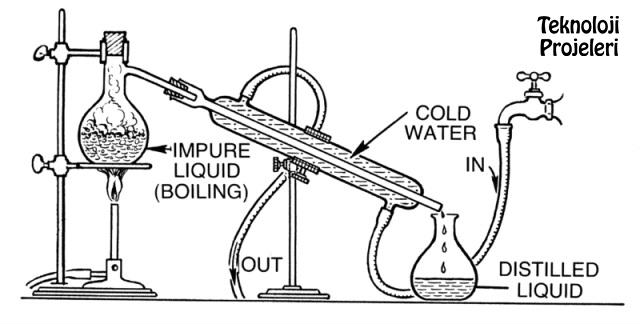
Destilasyon Nasıl Yapılır?
İşlem için öncelikli olarak karışımın ısıtılması sağlanır. Böylelikle buhar veya sıvı faz oluşumu elde edilir ve ardından uçucu özelliği kullanılır. Buhar faz sürecinde uçucu özelliği çok daha fazla olan ilk bileşen zenginleşirken sıvı fazda ise tam tersi bir durum görülür. Kaynama noktası itibariyle seviyesi daha yüksek olan ikinci bileşim sıvı faz sonucu zengin hale gelir. Buna karşın işlemlerde buhar ve sıvı faz bileşimlerinin aynı düzeyde olması halinde ise yapılan destilasyon işleminde istenen düzeyde ayırma gerçekleşmesi söz konusu değildir. Yapılma durumlarıyla birlikte çalışma şeklinde göre de destilasyon türleri sıralanabilir. Sürekli ya da kesikli işlemler yapılabileceği gibi besleme akımına göre de çoklu sistem-ikili sistem ayrımı vardır. Tek akım ya da çok akım ise elde edilen ürün akımına göre destilasyon çeşitlerinin sınıflandırılmasını gösterir.

Ayrıca Bakınız: Louis Pasteur Kimdir? Hayatı, Buluşları Nelerdir?
Destilasyon Türleri Nelerdir?
İki farklı maddenin bulunması ve bu maddelerin kaynama noktalarının birbirine yakın olması durumunda Fraksiyonlu destilasyon uygulanır. Böylelikle ayrım istenilen seviyeye yakın bir hal kazanır. Kaynama sıcaklığına yakın seviyelerde bozunma olmayan maddelerin tümü için ise normal destilasyon yapılması en iyi seçimdir. Uçucu olma özelliğine sahip olmayan karışımlardan suda çözünmeyen maddeleri ayırmak amacıyla su buharı destilasyon işlemi kullanılır. Kaynama sıcaklığının üstüne çıkması ya da altta kalmasının bir önemi yoktur. Katı maddeler için geçerli olan bir başka destilasyon türü olarak öne çıkan kuru destilasyon ise dikkatli bir şekilde yapılmalıdır. Katı maddelerin ısıyı iletme sorunlarının oluşması ihtimali vardır. Ayrıca maddelerin parçalanması sonucunda ise istenilen durumun elde edilmesi zorlaşır. Kaynama sıcaklıklarının daha altında bir seviyede bozunma durumu olan maddeler için ise vakum destilasyon kullanılır.



